
当前课程知识点:基础生物化学实验 > 第四章 酶活力的测定 > 第三节 酶米氏常数的测定 > 菠萝蛋白酶米氏常数的计算(Folin酚法)
1. 顺利完成了菠萝蛋白酶米氏常数的测定实验后,我们得到了一系列的实验数据,

而且同学们已经学习过双倒数作图法计算米氏常数KM的思路和注意事项,所以请你自己练习用这组数据计算一下菠萝蛋白酶的米氏常数KM。接下来,我们一起来看看,你的计算过程和结果与我们的计算过程是否一致吧。
米氏方程双倒数作图的公式是
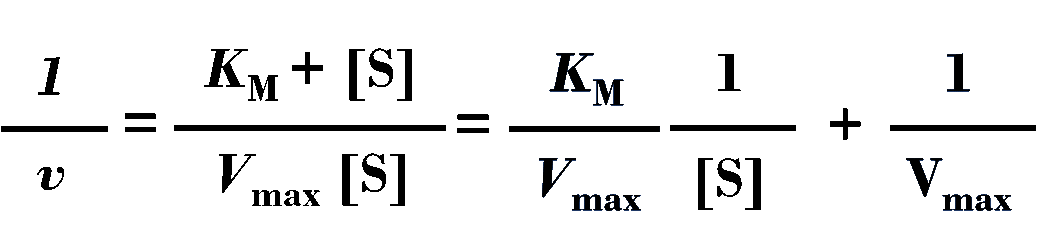
需要用1/[S]为横坐标,以1/v为纵坐标作图,所以我们要分别计算每支酶反应管里的底物浓度[S]和反应速度v。
2. 我们先来计算每支酶反应管里的反应速度,也就是每支管中每分钟生成酪氨酸的浓度,要知道各管中的酪氨酸的浓度,第一步,先要计算酪氨酸标准曲线浓度

3. 绘制酪氨酸浓度标准曲线
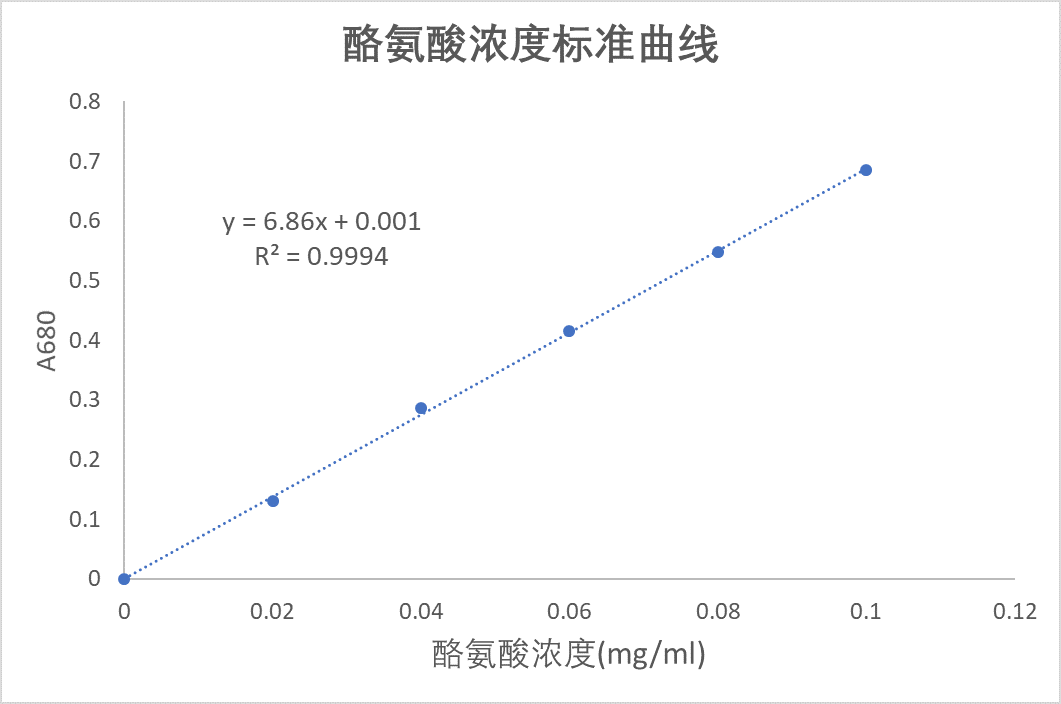
4. 接下来,计算不同底物浓度的酶反应管中在酶促反应时间生成的产物吸光度,也就是用各测定管的吸光度值减去空白管的吸光度值。
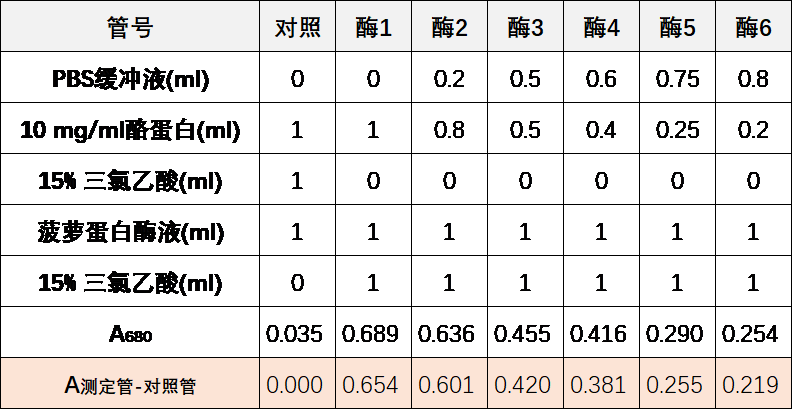
5. 利用酪氨酸浓度标准曲线的拟合方程,计算出各酶反应管中生成的酪氨酸浓度
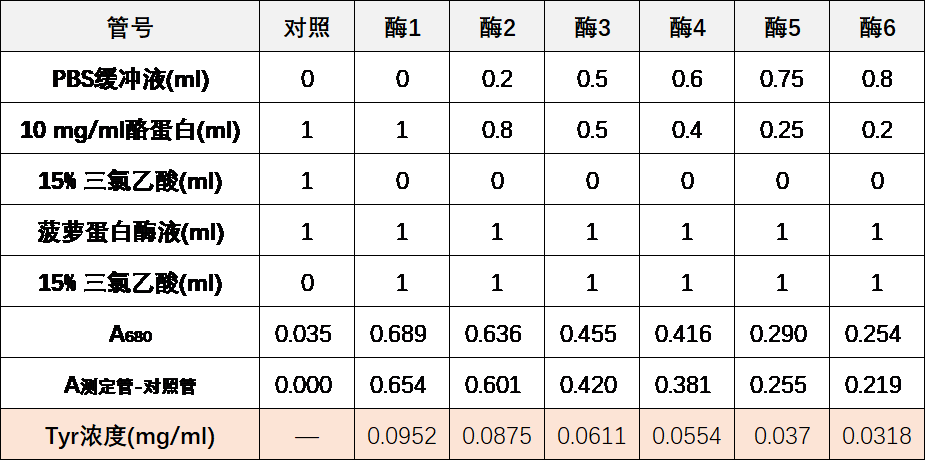
6. 接下来,我们需要计算各酶反应管中的反应速度,反应速度应该是每分钟生成酪氨酸的浓度,请注意,这里关键的问题是,计算哪个体系中的酪氨酸浓度?
是缓冲液+酪蛋白+酶液的2 ml体系,还是缓冲液+酪蛋白+酶液+三氯乙酸的3 ml体系呢?
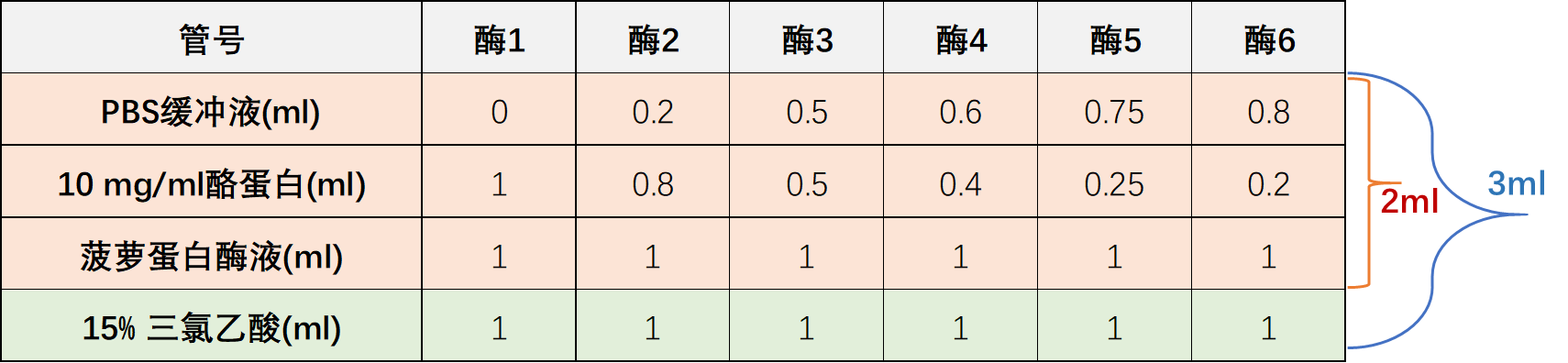
我们在前面的学习中已经详细讨论过,应该计算缓冲液+酪蛋白+酶液的“酶反应体系”,也就是2ml体系中的酪氨酸浓度。
7. 而我们现在算出的这些酪氨酸浓度是缓冲液+酪蛋白+酶液+三氯乙酸的3 ml“测定体系”中的酪氨酸浓度,所以这些数值还需要乘以3/2,换算成2 ml“酶反应体系”中的浓度,并除以反应时间10 min,得出各酶反应管的反应速度,并进而计算出各管中的1/v。
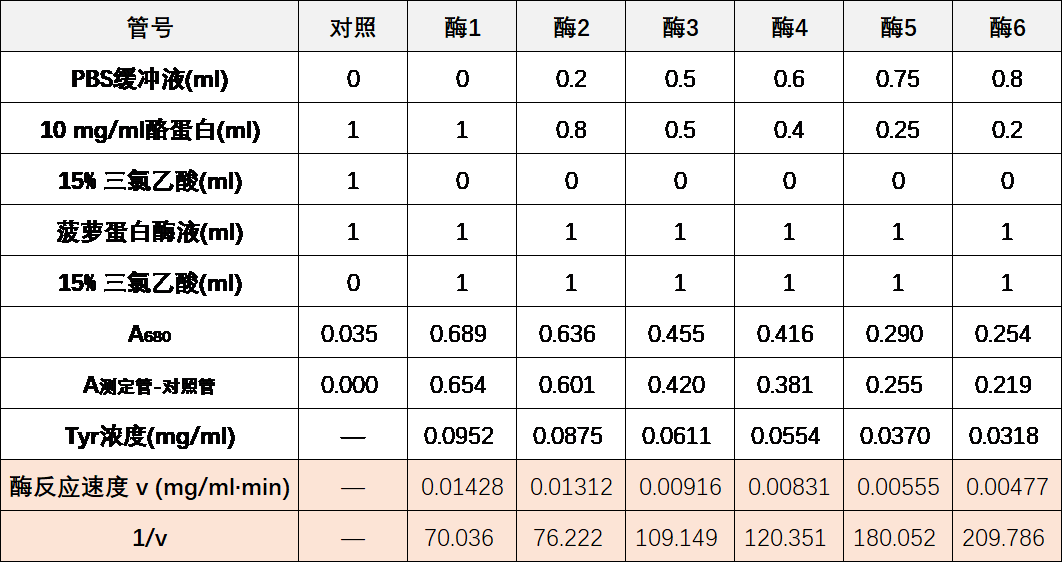
8. 此时,我们还需要各酶反应管中的底物浓度,浓度计算的步骤很简单,不过需要确定的是,这个底物浓度不是初始加入的底物浓度,而是2 ml“酶反应体系”中的底物浓度,所以我们需要将初始加入底物的体积乘以10 mg/ml的浓度,再除以2 ml酶反应体系体积,即可得到各酶促反应管中底物的浓度[S],进而计算出1/[S]。
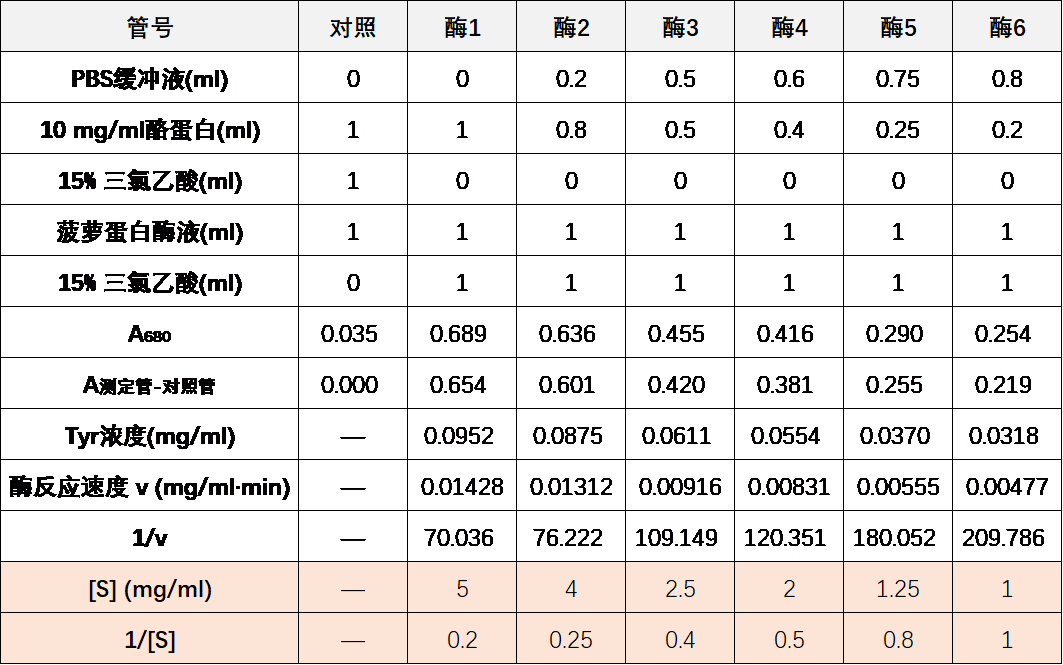
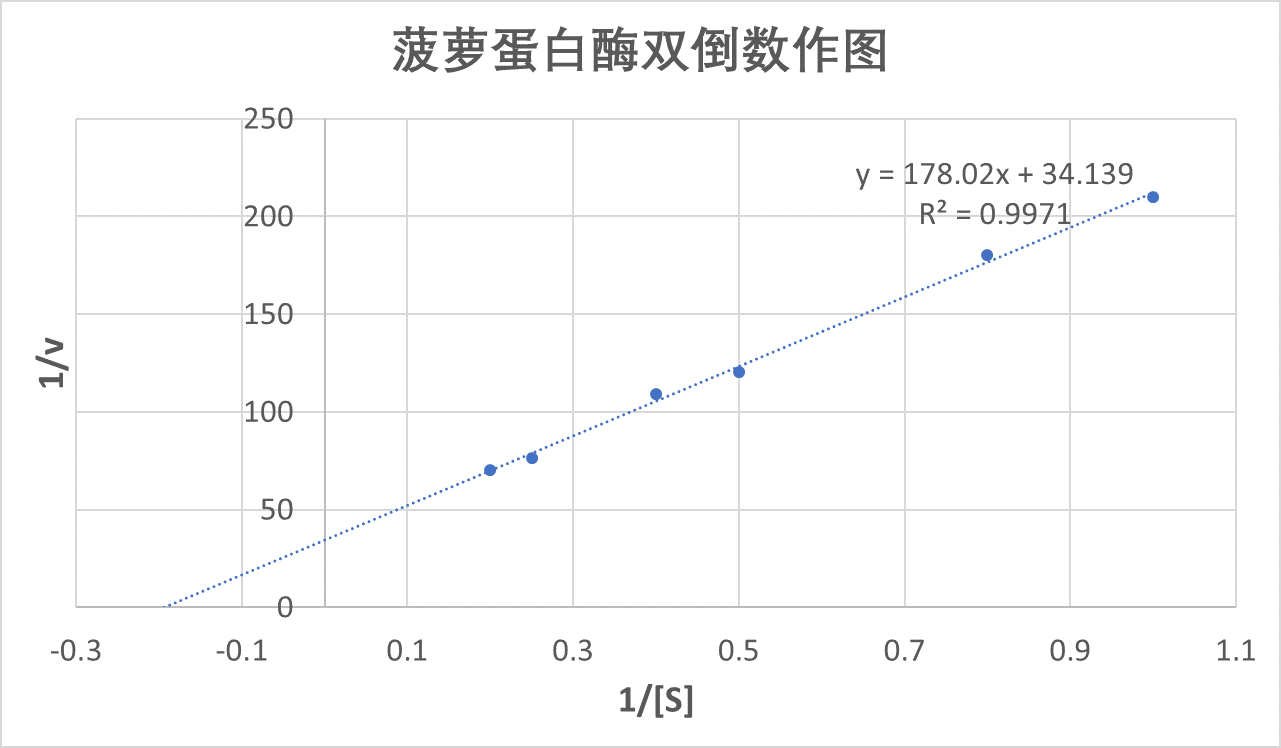
9. 以1/[S]为横坐标,以1/v为纵坐标,绘制双倒数图
10. 我们知道,米氏方程可以写成这种双倒数的形式
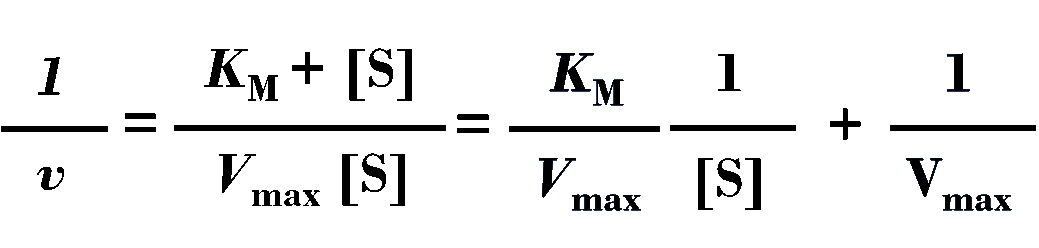
我们以1/[S]为横坐标,以1/v为纵坐标绘制的曲线其斜率就等于KM/Vmax,而曲线的纵截距即为1/Vmax,所以,我们的拟合方程中截距34.139 = 1/Vmax,
由此可以计算出Vmax = 1÷截距 = 1/34.139 = 0.029 mg/ml·min,
KM = 斜率÷截距 = 178.02 ÷ 34.139 = 5.215 mg/ml。
11. 好了,计算完了,和你算的一样吗?
-第一节 基础生物化学实验学什么?
-第二节 本课程评分标准
--本课程评分标准
-第三节 如何更好的完成本课程的学习?
-第四节 生化实验室安全注意事项
-第五节 本课程教学团队介绍
--本课程团队介绍
-第六节 课前须知作业
-第一章 课前须知 作业
-第一节 移液器的设计原理和使用规范
-第二节 移液器的操作要点
--移液器的操作要点
--移液器的操作要点
--移液器的日常校准
--移液器的日常校准
-第二章 移液器的使用 作业
--第二章 移液器的使用 作业
-第三节 分光光度计的设计原理和使用规范
-第四节 分光光度计的操作要点
-第五节 分光光度法测定待测物浓度
--分光光度法的原理
--分光光度法的原理
-第六节 荧光分光光度计的原理和使用规范
-第二章 分光光度计的使用 作业
--第二章 分光光度计的使用 作业
-第七节 离心机的设计原理和使用规范
--离心机的操作要点
--离心机的操作要点
-第二章 离心机的使用 作业
--第二章 离心机的使用 作业
-第一节 蛋白质的定量测定
-第三节 其他物质的测定
-第三章 物质的定量测定 作业
--第三章 物质的定量测定 作业
-第一节 酶活力测定的常用方法
-第二节 菠萝蛋白酶活力的测定
-第三节 酶米氏常数的测定
-第四章 酶活力的测定 作业
--第四章 酶活力的测定 作业
-第一节 蛋白质分离纯化的常见技术
--蛋白质的盐析提纯
--蛋白质的盐析提纯
--盐析操作注意事项
--盐析操作注意事项
--离子交换层析
--离子交换层析
--亲和层析
--亲和层析
--IMAC亲和层析
--IMAC亲和层析
--第五章 第一节 蛋白质的分离纯化 作业
-第二节 核酸的提取和检测
--第五章 第二节 核酸的提取 作业
-第一节 核酸琼脂糖凝胶电泳
--核酸琼脂糖电泳-作业
-第二节 聚丙烯酰胺凝胶电泳
--SDS-PAGE的原理和操作-作业
-《基础生物化学实验》期末考试


